产品合规
备案/注册/咨询/培训
近期,泰国食品药品监督管理局(Thai FDA)发布了一张关于微针类化妆品监管要求的官方科普图,引发行业广泛关注。
这张图的核心目的只有一个:明确哪些微针可以作为化妆品上市,哪些绝对不行。
为了帮助企业快速理解政策要点,我们将官方内容拆解成最关键的四部分:产品分类、合规要求、处罚标准与企业行动指南。
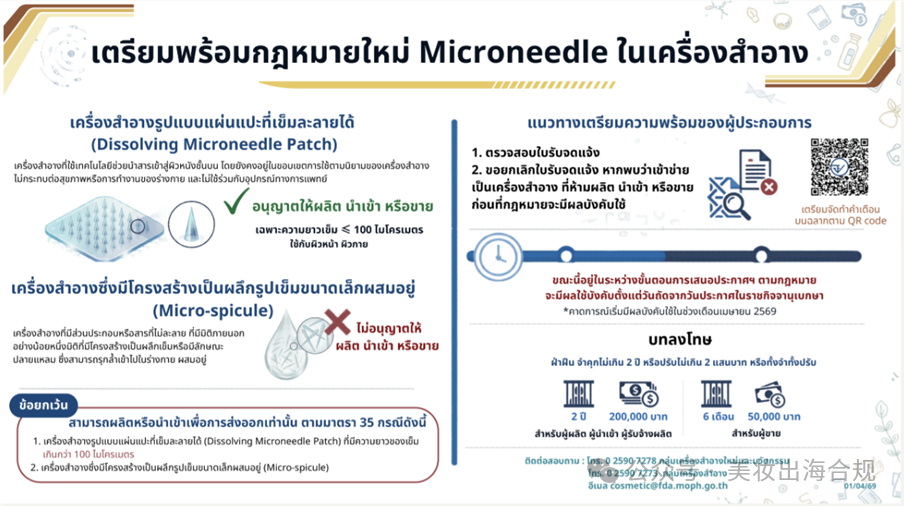
一、两类微针产品的监管分界线
定义:针体可完全溶解、以贴片形式使用的微针产品。
监管要求包括:
针长 ≤ 100 微米(0.1 mm),仅作用于皮肤表层
不得宣称任何医疗功效(如治疗、医美、修复组织等)
可按普通化妆品进行申报与上市
法规依据:泰国《化妆品法》第35条
一句话总结:只要是可溶、针长不超过100μm、无医疗宣传,就能作为化妆品。
2. 不可溶微针 / 微晶(Micro-spicule)——禁止作为化妆品
定义:针体由不可溶材料制成,如硅、玻璃、矿物晶体、植物硬刺等。
监管判定:
无论针长多少,一律不能作为化妆品上市
直接被归类为医疗器械
不得以化妆品名义宣传或销售
一句话总结:不可溶微针完全被禁止作为化妆品。
二、企业必须完成的三项合规准备
1. 产品类别自查
1)是否属于可溶微针
2)针长是否 ≤100μm
3)是否涉及不可溶晶体结构
2. 宣传内容全面排查
1)禁止出现“治疗、修复、医美、淡疤、祛皱”等医疗暗示
2)违规宣传将直接按化妆品法处罚
3. 合规时间节点
1)泰国FDA已设定过渡期
2)预计将于2026年4月开始生效
3)逾期未整改将全面执法
三、违规处罚标准(泰国本地法规)
违规主体 | 处罚措施 |
生产商 / 进口商 / 经销商 | 最高 2 年监禁 + 20 万泰铢罚款 |
普通销售者(零售商) | 最高 6 个月监禁 + 5 万泰铢罚款 |
四、简化版合规总结
产品类型 | 合规性 | 核心要求 | 违规后果 |
可溶微针贴片 | ✅ 合规 | 针长≤100μm,无医疗宣传,按普通化妆品申报 | 违规宣传按化妆品法处罚 |
不可溶微晶 / 微针 | ❌ 禁止 | 不得作为化妆品上市,仅可按医疗器械申报 | 直接按非法化妆品处罚,最高 2 年监禁 + 20 万泰铢罚款 |