产品合规
备案/注册/咨询/培训
2025年上半年,中国化妆品新原料备案以平均每周3款的速度狂飙突进!截至2025年6月18日,国家药监局公示的新原料数量达到75款,这一数据较2024年同期暴增74%,创下历史新高。以目前的增长速度,可能9月前就能达到2024年全年的新原料备案数量。
75款备案公示的新原料中,国产原料占比近九成,“中国成分”的领跑格局已然成型。中国特色植物原料遥遥领先,肽类原料增长迅猛,生物技术原料欣欣向荣。
政策驱动:备案狂飙的“推手”
2021年,国家药监局发布《化妆品新原料注册备案资料管理规定》,奠定了新原料申报的基础。2021年新原料备案数量仅为6款,2022年新原料备案数量增长至42款,2023年增长至69款,2024年增长至90款。新原料备案数量每年增长背后,是越来越明确的申报要求以及越来越多的政策指引。
政策明晰化与服务体系升级直接驱动备案激增:2021年新规实施后,新原料备案数量从年备案6款飙升至2024年90款,4年增长14倍。这一爆发式增长的核心动能,源于国家药监局通过技术指南(如申报情形界定、判定)明确申报边界,以及政策工具箱扩容——从《支持化妆品原料创新若干定》的毒理试验减免,到中检院“技术问答+沟通机制”及时解疑,系统性降低企业研发申报的不确定性。
2023年,中检院发布《化妆品新原料沟通交流工作机制(试行)》的通知,促进了新原料注册人、备案人与化妆品技术审评部门之间的沟通交流;2024年,中检院发布《化妆品新原料常见技术问答》,明确了新原料资料填报要求;2025年,国家药监局发布关于支持化妆品原料创新若干规定的公告,旨在完善化妆品创新发展机制,优化原料管理措施和技术要求。同时,中检院还发布了化妆品新原料判定、新原料界定、安全使用历史、安全食用历史等一系列技术指南的征求意见稿,并开展了新原料技术培训课程。
表1 国家药监局、中检院发布的新原料相关的法规或政策
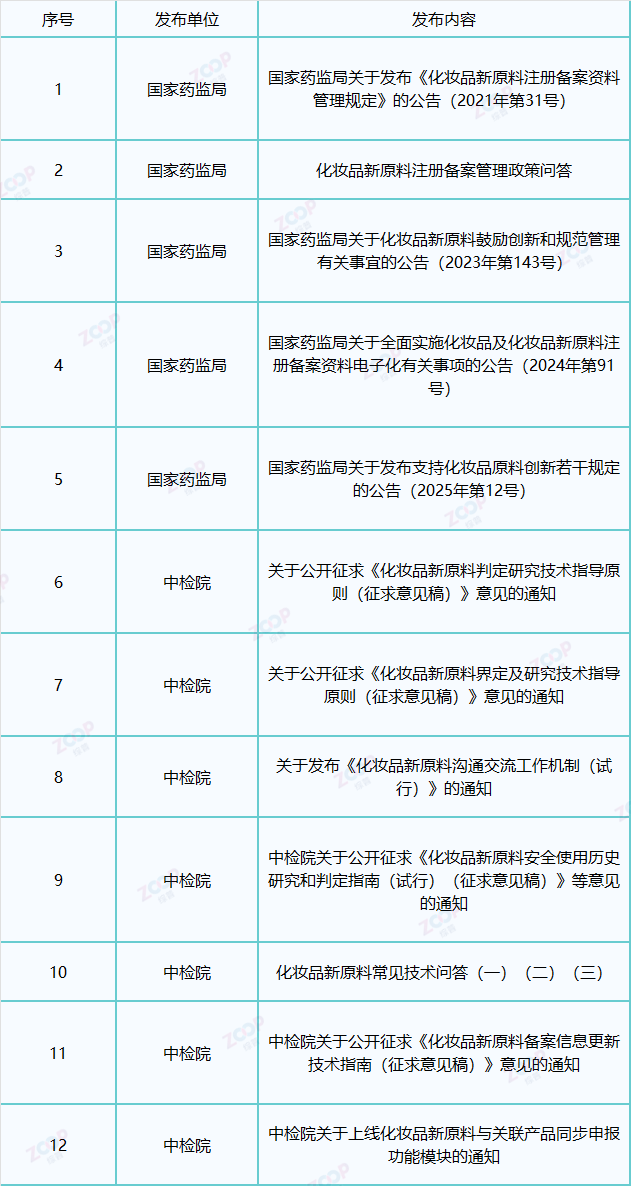
《化妆品监督管理条例》明确:鼓励和支持运用现代科学技术,结合我国传统优势项目和特色植物资源研究开发化妆品。
广东、上海两地以全国近50%的新原料备案量领跑全国,全国首个注册新原料于2024年落地上海,政策红利精准滴灌+创新生态厚植土壤,双轮驱动行业高地加速崛起。
广东、上海密集出台专项扶持政策,构建多维度支持体系:对纳入《已使用化妆品原料目录》的新原料给予资金扶持(如广州对企业累计最高扶持500万元);按产业化营收规模给予梯度扶持(如广州对企业最高扶持150万元);重点倾斜合成生物技术及特色植物资源开发(如深圳对中国特色植物原料补贴高达200万元);上海设立工作专班实现5日内快速响应企业咨询。
技术创新:中国特色原料的“秘籍”
随着《化妆品监督管理条例》及配套政策深化实施,我国植物类化妆品新原料备案呈现爆发式增长。今年植物新原料备案数量占今年新原料备案总量近三分之一,多于2021年至2023年植物新原料备案数量总和,和2024年植物新原料备案数量基本持平。这一现象背后,是以中国特色资源开发为根基、以技术创新为引擎的产业升级路径。其核心特征可归纳为五大方向:
一、深耕中国特色资源,构建地域品牌护城河
政策明确鼓励开发传统优势植物资源,推动企业聚焦地域性珍稀物种,形成原料差异化壁垒:广西倚靠被誉为“植物界大熊猫”的珍惜植物金花茶,开发出金花茶花提取物和金花茶叶提取物;云南发掘多种高原/山地环境下生长的珍惜植物,如滇牡丹、球药隔重楼、南方红豆杉;更有植物物种名称自带地理区域,如天山雪莲、岷江蓝雪花、东北刺参、浙江红山茶等,尽显地方特色。

金花茶
二、资源开发多维化,破解可持续供应瓶颈
同种植物不同部位的组成含量有所不同,企业通过植物部位精细化开发,实现从同种植物到多种化妆品原料的应用,打造差异化植物原料;巧用植物愈伤组织、培养物技术开发化妆品原料(如昙花愈伤组织提取物、铁皮石斛培养物),提升了资源利用率。
三、活性成分提纯,提升功效合规双效性
锚定植物中的活性成分(如红景天中的红景天苷,长梗冬青中的长梗冬青苷),制备高纯度成分,研究其功效机制,并以结构明确的单一化合物的形式申报化妆品新原料,减少了申报的不确定性。

红景天
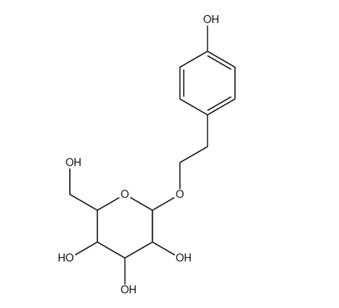
红景天苷
四、生物技术赋能增效,突破天然提取物局限
合成生物学与发酵工程推动植物原料升级:以植物原料为底物,通过菌株代谢提升植物活性物质含量;基于合成生物学技术构建的“细胞工厂”,通过微生物全细胞催化体系,实现了连续发酵产出高纯度植物活性成分,降低了生产成本。
五、跨领域应用拓展,复用安全数据降本提速
具有安全食用历史的植物原料凭借成熟安全的数据加速其向化妆品转化:从传统药材到“药食同源”,从“药食同源”转向“妆食同源”,植物原料以其安全性实现了从食品到化妆品的跨界应用。具有安全食用历史的原料可豁免系统毒理测试,也很大程度减少了企业申报化妆品新原料的成本和周期,加速了原料在化妆品的应用。
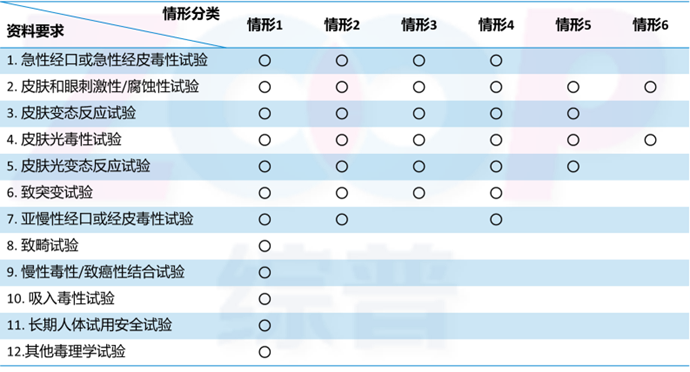
情形5:具有安全食用历史的化妆品新原料应提交的毒理学试验较少
合规研究:新原料申报的“安全带”

申报系统后台显示备案后技术核查意见
国家药监局数据查询平台显示,有多款化妆品新原料的状态显示为“已注销”,详情显示“该原料为已使用的化妆品原料,不按新原料管理。”这也提示新原料备案人,在新原料立项前,应仔细研判拟申报原料是否在新原料备案范畴,避免备案后“竹篮打水一场空”。
新原料需在3年安全监测期内提交年度报告,新原料备案人、注册人应收集新原料使用的相关信息,汇总原料生产、销售情况和新原料不良反应监测情况。化妆品新原料安全监测期满3年后,技术审评机构应当向国家药品监督管理局提出化妆品新原料是否符合安全性要求的意见,对存在安全问题的化妆品新原料,由国家药品监督管理局撤销注册或者取消备案;未发生安全问题的,由国家药品监督管理局纳入已使用的化妆品原料目录。
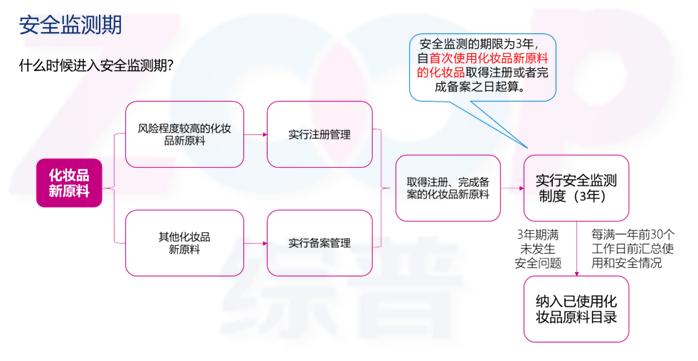
安全监测期的计算
首个完成备案的化妆品新原料N-乙酰神经氨酸(备案编号:国妆原备字20210001),从进入监测期到现在已满3年,可以预见该原料可能被收录到《已使用化妆品原料目录》中。届时原料以什么形式纳入《已使用化妆品原料目录》,原料是否应遵循技术要求,安全监测期内同名称的其他原料如何管理,这些问题也将成为行业关注点。
化妆品新原料从立项研发到终端应用的全生命周期中,合规管理需贯穿始终。在立项阶段,企业需精准界定原料是否属于新原料,合理选择申报情形,规避研发方向性风险;研发阶段需把握质量规格指标,控制杂质含量;检测阶段需确保检测有法可依;安全评估环节须确保数据真实完整,评估过程科学严谨;进入备案注册阶段,应按法规要求提交完整资料;监测期管理(3年)是持续合规的关键,注册/备案人需建立安全预警体系,每年报告使用情况,及时响应不良反应信号,关注技术审评意见进展。

中国化妆品新原料正以每周3款的速度重构全球创新版图,这一增长主要受益于政策精准支持与技术突破的双重作用,当前仍需破解同质化竞争困局,通过特色资源开发和核心技术壁垒构建,推动备案优势转化为市场竞争力,通过强化基础研究,实现从“数量增长”向“技术话语权”的升级。
综普的新原料服务
◆ 辅导新原料注册人、备案人建立安全风险监测和评价体系;
◆ 根据提供的新原料基本信息、研发背景、最新研究进展,协助完成新原料研制报告编写;
◆ 指导申请人编制新原料制备工艺;
◆ 指导申请人编制质量控制标准,包括稳定性试验数据、质量规格指标及其检验方法、可能存在的安全性风险物质及其控制资料;
◆ 指导申请人对新原料进行毒理学试验并编制毒理学安全性评价资料;
◆ 收集新原料功效依据的相关资料,包括科学文献、法规资料、体外或动物试验研究数据、人体功效评价资料等;
◆ 指导申请人编制新原料技术要求;
◆ 指导申请人编制化妆品新原料安全监测年度报告;
◆ 新原料注册、备案全程代理专业服务。