产品合规
检测/备案/注册
目录-------------------
一、法规背景介绍
二、用户信息新要求
三、注册与备案资料新要求
(一)注册/备案申请表
(二)产品名称命名依据
(三)产品配方
(四)产品执行的标准
(五)产品标签
(六)产品检验报告
(七)产品安全评估资料
一、法规背景介绍
2020年6月《化妆品监督管理条例》发布,化妆品的监管进入新时代。
按照新的化妆品定义和分类,化妆品分为特殊化妆品与普通化妆品。
国家对特殊化妆品实行注册管理,对普通化妆品实行备案管理。
化妆品注册人、备案人对化妆品的质量安全和功效宣称负责。
《化妆品监督管理条例》
对本条例施行前已经注册的用于育发、脱毛、美乳、健美、除臭的化妆品自本条例施行之日起设置5年的过渡期,过渡期内可以继续生产、进口、销售,过渡期满后不得生产、进口、销售该化妆品。
牙膏参照本条例有关普通化妆品的规定进行管理。牙膏备案人按照国家标准、行业标准进行功效评价后,可以宣称牙膏具有防龋、抑牙菌斑、抗牙本质敏感、减轻牙龈问题等功效。牙膏的具体管理办法由国务院药品监督管理部门拟订,报国务院市场监督管理部门审核、发布。(暂未出台)
香皂不适用本条例,但是宣称具有特殊化妆品功效的适用本条例。
《化妆品监督管理条例》颁布之后,国家市场监督管理总局、国家药品监督管理局于2021年相继颁布了以下配套法规,保障新条例下化妆品注册与备案的施行。
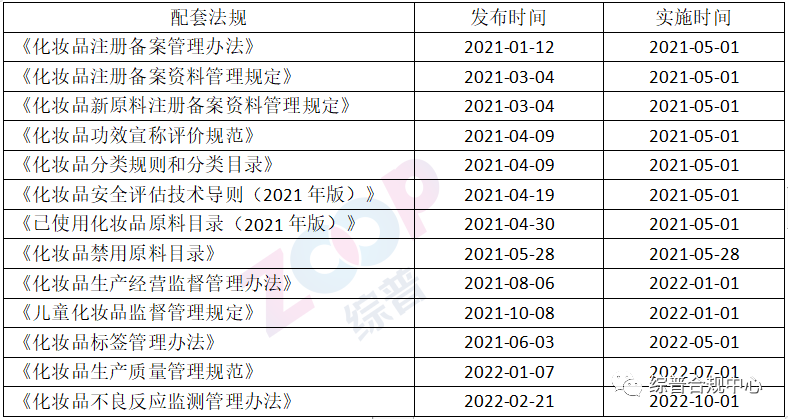
二、用户信息新要求
《化妆品监督管理条例》第十八条
《化妆品注册备案管理办法》第二十八条
化妆品注册申请人、备案人应当具备下列条件:
(一)是依法设立的企业或者其他组织;
(二)有与申请注册、进行备案的产品相适应的质量管理体系;
(三)有化妆品不良反应监测与评价能力。
注册申请人首次申请特殊化妆品注册或者备案人首次进行普通化妆品备案的,应当提交其符合前款规定要求的证明资料。
《化妆品注册备案资料管理规定》
第二章 用户信息相关资料要求
第一节 资料项目及要求
第十条 首次申请特殊化妆品注册或者办理普通化妆品备案时,境内的注册申请人、备案人和境内责任人应当提交以下用户信息相关资料:
(一)注册人备案人信息表及质量安全负责人简历;
(质量安全负责人的简历应当包括与其要求相关的教育背景、工作经历以及其他内容)
(《化妆品监督管理条例》第三十二条 化妆品注册人、备案人、受托生产企业应当设质量安全负责人,承担相应的产品质量安全管理和产品放行职责。)
质量安全负责人的任职要求:质量安全负责人应当具备化妆品、化学、化工、生物、医学、药学、食品、公共卫生或者法学等化妆品质量安全相关专业知识和法律知识,熟悉相关法律、法规、规章、强制性国家标准、技术规范,并具有5年以上化妆品生产或者质量管理经验。

(二)注册人备案人质量管理体系概述;
质量管理体系概述是对注册人、备案人质量管理控制能力和过程的总结描述,应当如实客观地反映实际情况,包括供应商遴选、原料验收、生产及质量控制、产品留样等管理制度。语言应当简明扼要,体现出质量控制关键点设置和日常执行管理要求。
注册人、备案人同时存在自行生产和委托生产的,应当分别提交相应版本的质量管理体系概述。


(三)注册人备案人不良反应监测和评价体系概述;
不良反应监测和评价体系概述是对注册人、备案人和境内责任人不良反应监测评价能力和过程的总结描述,应当如实客观地反映实际情况。语言应当简明扼要,体现出不良反应监测关键点、各环节设置和日常执行管理要求。

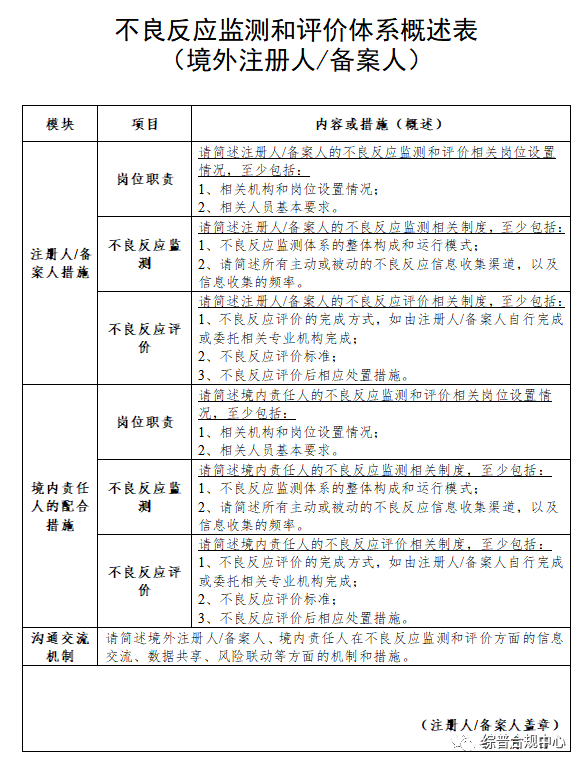
(四)境外注册人、备案人应当提交境内责任人信息表;
《化妆品注册备案管理办法》
第八条 注册人、备案人在境外的,应当指定我国境内的企业法人作为境内责任人。境内责任人应当履行以下义务:
(一)以注册人、备案人的名义,办理化妆品、化妆品新原料注册、备案;
(二)协助注册人、备案人开展化妆品不良反应监测、化妆品新原料安全监测与报告工作;
(三)协助注册人、备案人实施化妆品、化妆品新原料召回工作;
(四)按照与注册人、备案人的协议,对投放境内市场的化妆品、化妆品新原料承担相应的质量安全责任;
(五)配合药品监督管理部门的监督检查工作。

(五)境内责任人授权书原件及其公证书原件;
《化妆品注册备案资料管理规定》
第五条 化妆品注册备案资料应当符合国家有关用章规定,签章齐全,具有法律效力。境外企业及其他组织不使用公章的,应当由法定代表人或者企业(其他组织)负责人签字。除用户信息相关资料外,产品的注册备案资料中如需境外化妆品注册人、备案人签章的,其法定代表人或者负责人可授权该注册人、备案人或者境内责任人的签字人签字。授权委托签字的,应当提交授权委托书原件及其公证书原件,授权委托书中应当写明授权签字的事项和范围。
(六)注册人、备案人有自行生产或者委托境外生产企业生产的,应当提交生产企业信息表和质量安全负责人信息,一次性填报已有生产企业及其信息。生产企业为境外的,应当提交境外生产规范证明资料原件。
(无法提供证明资料原件的,应当提供由中国公证机关公证的或由我国使(领)馆确认的复印件。)
境外生产规范证明资料
境外生产企业应当提交生产企业符合质量管理体系或者生产质量管理规范的资质证书、文件等证明资料,证明资料应当由所在国(地区)政府主管部门、认证机构或者具有所在国(地区)认证认可资质的第三方出具或者认可,载明生产企业名称和实际生产地址信息。
境外生产质量管理规范证明资料有有效期限的,应当及时更新证明资料,最长不得超过有效期限截止后90日;无有效期限的,应当每五年提交最新版本。
三、注册与备案资料新要求


(一)注册/备案申请表
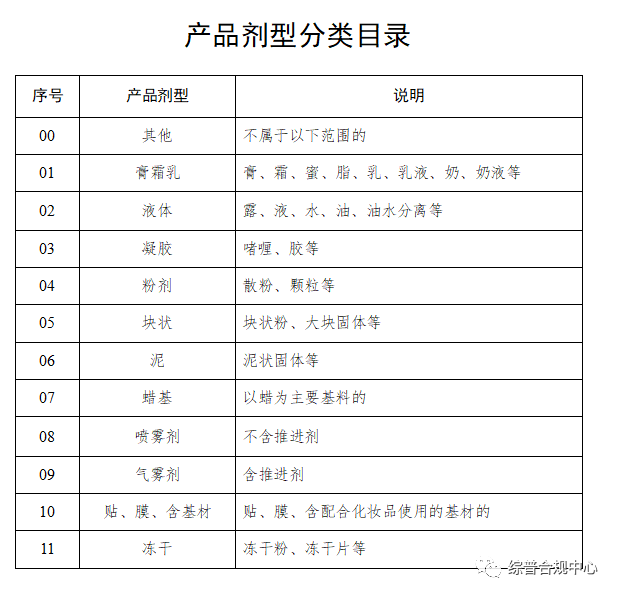
分类编码
注册人、备案人应当按照《化妆品监督管理条例》和化妆品分类规则与分类目录的规定,确定产品类别以及相应的产品分类编码,涉及特殊化妆品功效宣称的,应当按照特殊化妆品申报。
《化妆品监督管理条例》
第十六条 用于染发、烫发、祛斑美白、防晒、防脱发的化妆品以及宣称新功效的化妆品为特殊化妆品。特殊化妆品以外的化妆品为普通化妆品。
国务院药品监督管理部门根据化妆品的功效宣称、作用部位、产品剂型、使用人群等因素,制定、公布化妆品分类规则和分类目录。
《化妆品分类规则和分类目录》第三条 化妆品注册人、备案人应当根据化妆品功效宣称、作用部位、使用人群、产品剂型和使用方法,按照本规则和目录进行分类编码。

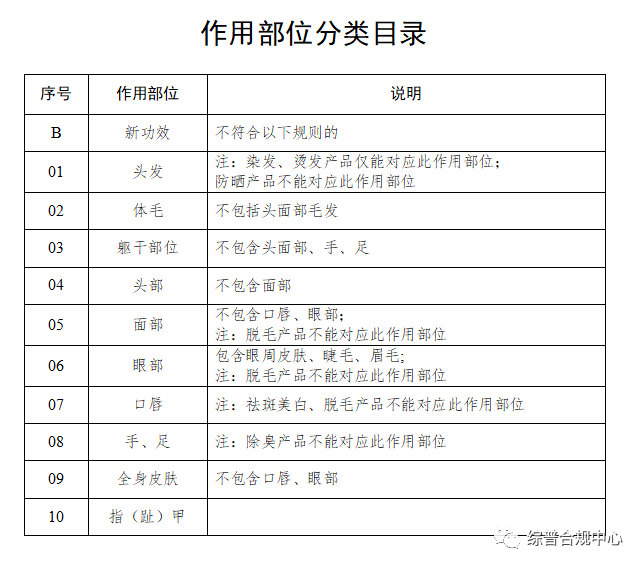
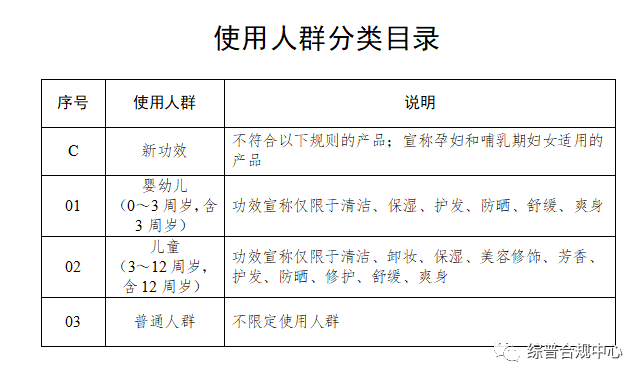

委托关系文件
委托境外企业生产的化妆品,注册人、备案人或者境内责任人应当提交委托关系文件。委托关系文件应当至少载明产品名称、委托方、受托生产企业名称、生产地址、本产品接受委托的日期、受托生产企业法人或者法人授权人的签章。注册人、备案人与受托生产企业属于同一集团公司的,可提交属于同一集团公司的证明资料以及企业集团出具的产品质量保证文件以确认委托关系。
自由销售证明
进口产品应当提供由化妆品注册人、备案人所在国或生产国(地区)政府主管部门或者行业协会等机构出具的已上市销售证明文件,境内注册人、备案人委托境外生产企业生产的和产品配方专为中国市场设计的除外。已上市销售证明文件应当至少载明注册人、备案人或者生产企业的名称、产品名称、出具文件的机构名称以及文件出具日期,并由机构签章确认。
1.组合包装产品同时存在进口部分和国产部分的,仅提交进口部分的已上市销售证明文件。
2.专为中国市场设计销售包装的,应当提交该产品在化妆品注册人、备案人所在国或生产国(地区)的已上市销售证明文件,同时提交产品配方、生产工艺与化妆品注册人、备案人所在国或者生产国(地区)产品一致的说明资料。
进口产品的已上市销售证明文件、委托关系文件或者属于一个集团公司的证明资料等文件可同时列明多个产品。这些产品申请注册或者办理备案时,其中一个产品可使用原件,其他产品可使用复印件,并说明原件所在的产品名称以及相关受理编号、注册证号或者备案编号等信息。
(二)产品名称命名依据
产品名称命名依据中应当指明商标名、通用名、属性名,并分别说明其具体含义。
进口产品应当对外文名称和中文名称分别进行说明,并说明中文名称与外文名称的对应关系(专为中国市场设计无外文名称的除外)。
注册商标需提供证明文件。产品中文名称中商标名使用字母、汉语拼音、数字、符号等的,应当提供商标注册证。
(三)产品配方
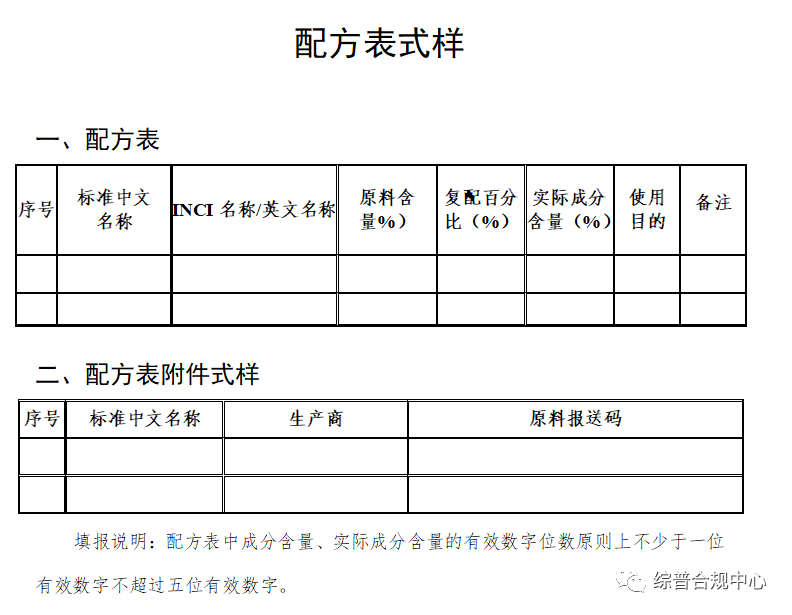
配方表要求:产品配方表应当包括原料序号、原料名称、百分含量、使用目的等内容。
原料名称
产品配方应当提供全部原料的名称,原料名称包括标准中文名称、国际化妆品原料名称(简称INCI名称)或者英文名称。配方成分的原料名称应当使用已使用的化妆品原料目录中载明的标准中文名称、INCI名称或者英文名称;
配方中含有尚在安全监测中化妆品新原料的,应当使用已注册或者备案的原料名称;进口产品原包装标注成分的INCI名称与配方成分名称不一致的,应当予以说明。
使用着色剂的,应当在产品配方原料名称栏中标明《化妆品安全技术规范》载明的着色剂索引号(简称CI号),无CI号的除外;使用着色剂为色淀的,应当在着色剂后标注“(色淀)”,并在配方备注栏中说明所用色淀的种类;
使用纳米原料的,应当在此类成分名称后标注“(纳米级)”。
百分含量
产品配方应当提供全部原料的含量,含量以质量百分比计,全部原料应当按含量递减顺序排列;含两种或者两种以上成分的原料(香精除外)应当列明组成成分及相应含量。
使用目的
应当根据原料在产品中的实际作用标注主要使用目的;申请祛斑美白、防晒、染发、烫发、防脱发的产品,应当在配方表使用目的栏中标注相应的功效成分,如果功效原料不是单一成分的,应当在配方表使用目的栏中明确其具体的功效成分。
备注栏
以下情形应当在备注栏中说明:
使用变性乙醇的,应当说明变性剂的名称及用量;
使用类别原料的,应当说明具体的原料名称;
直接来源于植物的,应当说明原植物的具体使用部位;
使用来源于石油、煤焦油的碳氢化合物(单一组分除外)的,应当在产品配方表备注栏中标明相关原料的化学文摘索引号(简称CAS号);
含有与产品内容物直接接触的推进剂的,应当在配方备注栏中标明推进剂的种类、添加量等。
原料信息、原料安全信息
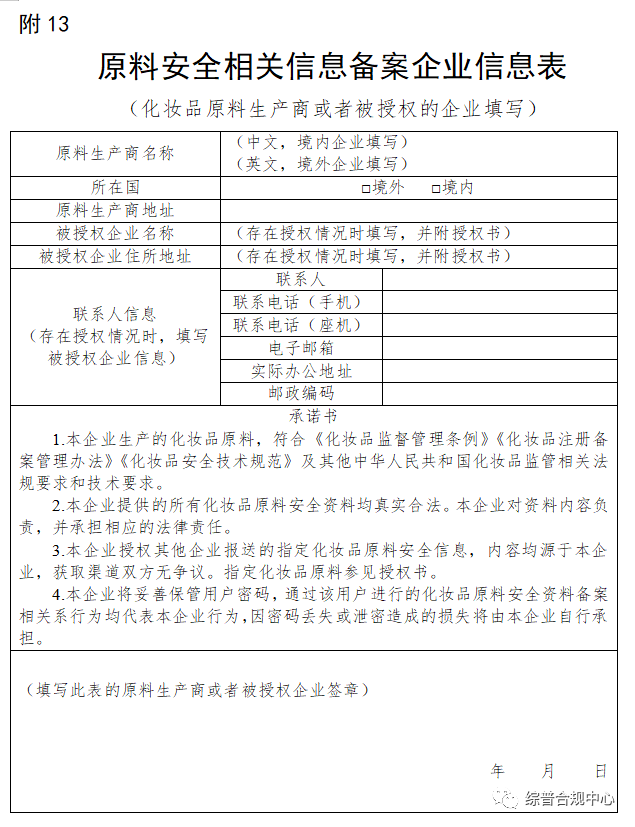
自2021年5月1日起,注册人备案人申请注册或者进行备案时,应当填报产品配方原料的商品名和生产商信息,
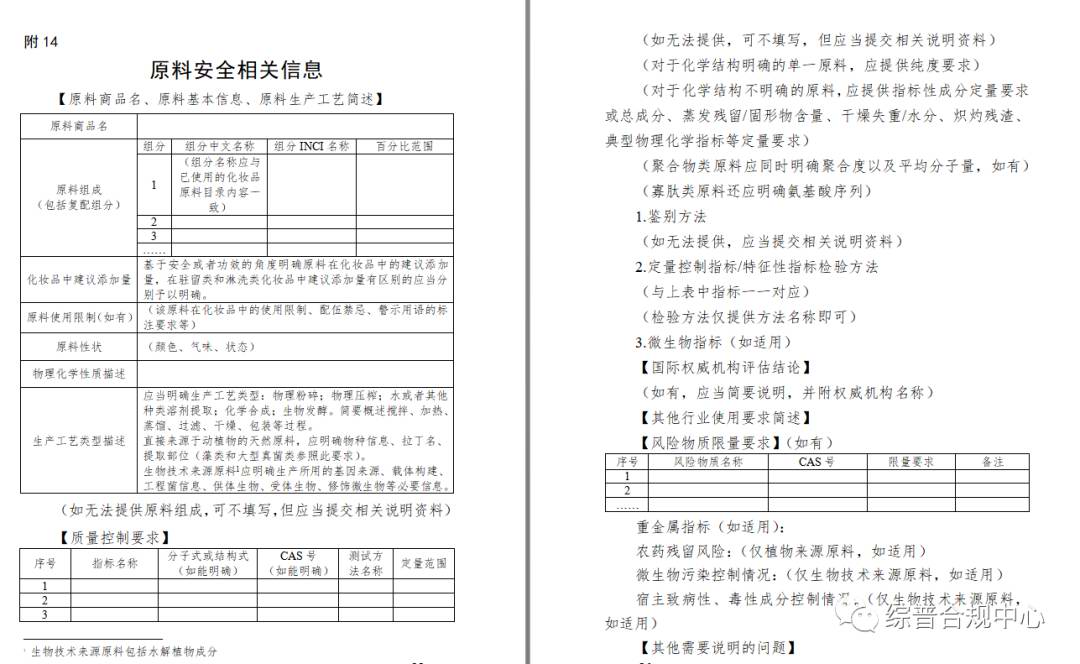
自2022年1月1日起,注册人备案人申请注册或者进行备案时,应当按照《规定》的要求,提供具有防腐、防晒、着色、染发、祛斑美白功能原料的安全相关信息。
自2023年1月1日起,注册人备案人申请注册或者进行备案时,应当按照《规定》的要求,提供全部原料的安全相关信息。此前已经取得注册或者完成备案的化妆品,注册人、备案人应当在2023年5月1日前补充提供产品配方中全部原料的安全相关信息。
化妆品新原料
使用了尚在安全监测中化妆品新原料的,注册人、备案人或者境内责任人应当经新原料注册人、备案人确认后,方可提交注册申请或者办理备案。
载体材料
使用贴、膜类载体材料的,应当在备注栏内注明主要载体材料的材质组成,同时提供其来源、制备工艺、质量控制指标等资料。
香精填写方式
产品配方香精可按两种方式填写,分别提交以下资料:
1.产品配方表中仅填写“香精”原料的,无须提交香精中具体香料组分的种类和含量;产品标签标识香精中的具体香料组分的,以及进口产品原包装标签标识含具体香料组分的,应当在配方表备注栏中说明。
2.产品配方表中同时填写“香精”及香精中的具体香料组分的,应当提交香精原料生产商出具的关于该香精所含全部香料组分种类及含量的资料。
动物脏器组织及血液制品
产品配方中使用动物脏器组织及血液制品提取物作为原料的,应当提供其来源、组成以及制备工艺,并提供原料生产国允许使用的相关文件。
(四)产品执行的标准
产品执行的标准包括全成分、生产工艺简述、感官指标、微生物和理化指标及其质量控制措施、使用方法、贮存条件、使用期限等内容,应当符合国家有关法律法规、强制性国家标准和技术规范的要求。
产品名称
包括中文名称和进口产品的外文名称。
全成分
包括生产该产品所使用的全部原料的序号、原料名称和使用目的,所有原料应当按含量递减顺序排列。
工艺简述
1.应当简要描述实际生产过程的主要步骤,包括投料、混合、灌装等。配方表2个以上原料的预混合、灌装等生产步骤在不同生产企业配合完成的,应当予以注明。
2.应当体现主要生产工艺参数范围,全部原料应当在生产步骤中明确列出,所用原料名称或者序号应当与产品配方中所列原料一致;若同一原料在不同步骤阶段中使用,应当予以区分;若生产过程中需使用但在后续生产步骤中去除的水、挥发性溶剂等助剂,应当予以注明。
感官指标
1.颜色是指产品内容物的客观色泽。
同一产品具有可区分的多种颜色,应当逐一描述;难以区分颜色的,可描述产品目视呈现或者使用时的主要色泽,也可描述颜色范围。
2.性状是指产品内容物的形态。
3.气味是指产品内容物是否有气味。(有香味、有原料特征性气味、无味)

套装产品应当分别说明各部分的感官指标。
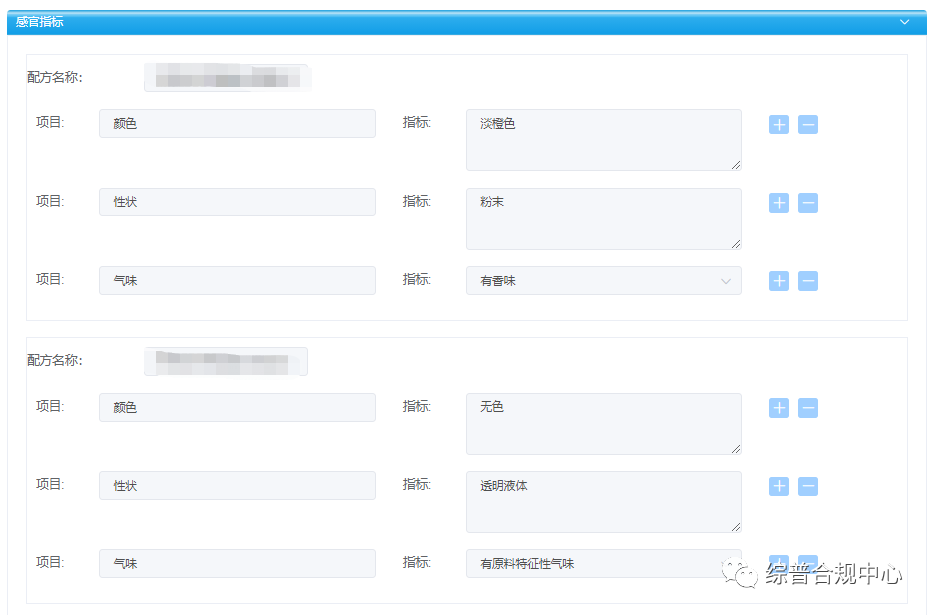
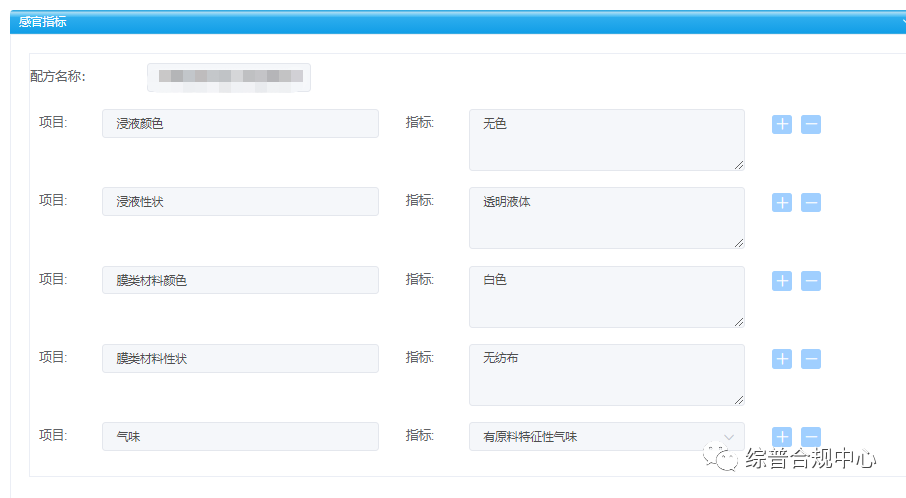
使用贴、膜类载体材料的产品应当分别描述贴、膜类材料以及浸液的颜色、性状等。
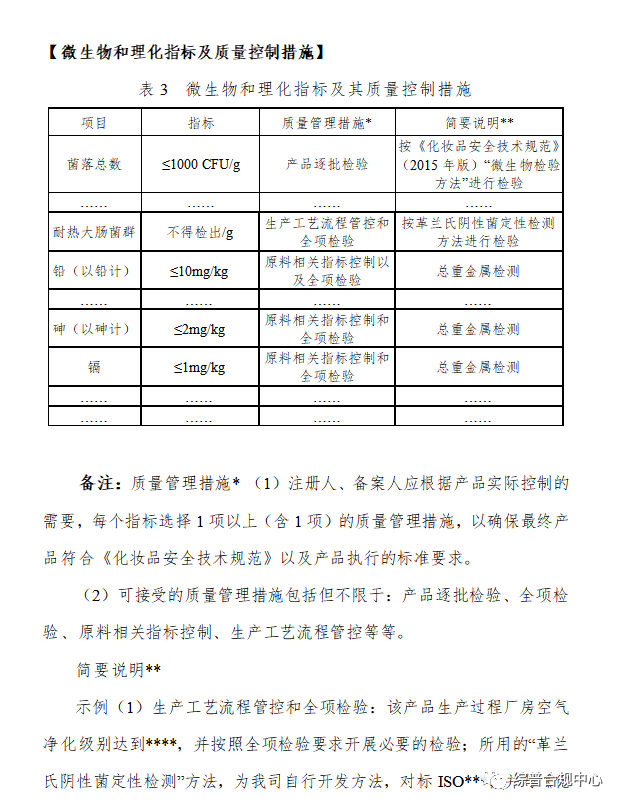
微生物和理化指标及质量控制措施
1.应当提交对产品实际控制的微生物和理化指标,微生物和理化指标应当符合《化妆品安全技术规范》《化妆品注册和备案检验工作规范》的要求。
2.应当根据产品实际控制的微生物和理化指标提交相应的质量控制措施。
3.采用检验方式作为质量控制措施的,应当注明检验频次,检验方法名称(所用方法与《化妆品安全技术规范》所载方法完全一致的,应当填写规范所载方法名称;不一致的应当填写经过验证的方法名,说明该方法是否与《化妆品安全技术规范》所载方法开展过验证,完整的检验方法和方法验证资料留档备查。)
4.采用非检验方式作为质量控制措施的,应当明确具体的实施方案,对质量控制措施的合理性进行说明,以确保产品符合《化妆品安全技术规范》要求。

使用方法
应当阐述化妆品的使用方法,对使用人群和使用部位有特殊要求的,应当予以说明;安全警示用语应当符合化妆品标签管理规定和《化妆品安全技术规范》等相关法规的要求。
贮存条件
应当根据产品包装及产品自身稳定性等特点设定产品贮存条件。
使用期限
应当根据产品包装、产品自身稳定性或者相关实验结果,设定产品的使用期限。
(五)产品标签
《化妆品监督管理条例》
第三十五条 化妆品的最小销售单元应当有标签。标签应当符合相关法律、行政法规、强制性国家标准,内容真实、完整、准确。
进口化妆品可以直接使用中文标签,也可以加贴中文标签;加贴中文标签的,中文标签内容应当与原标签内容一致。
《化妆品标签管理办法》
第五条 化妆品的最小销售单元应当有标签。标签应当符合相关法律、行政法规、部门规章、强制性国家标准和技术规范要求,标签内容应当合法、真实、完整、准确,并与产品注册或者备案的相关内容一致。
化妆品标签应当清晰、持久,易于辨认、识读,不得有印字脱落、粘贴不牢等现象。
《化妆品监督管理条例》
第三十六条 化妆品标签应当标注下列内容:
(一)产品名称、特殊化妆品注册证编号;
(二)注册人、备案人、受托生产企业的名称、地址;
(三)化妆品生产许可证编号;
(四)产品执行的标准编号;
(五)全成分;
(六)净含量;
(七)使用期限、使用方法以及必要的安全警示;
(八)法律、行政法规和强制性国家标准规定应当标注的其他内容。
《化妆品标签管理办法》第七条 化妆品中文标签应当至少包括以下内容:
(一)产品中文名称、特殊化妆品注册证书编号;
(二)注册人、备案人的名称、地址,注册人或者备案人为境外企业的,应当同时标注境内责任人的名称、地址;
(三)生产企业的名称、地址,国产化妆品应当同时标注生产企业生产许可证编号;
(四)产品执行的标准编号;
(五)全成分;
(六)净含量;
(七)使用期限;
(八)使用方法;
(九)必要的安全警示用语;
(十)法律、行政法规和强制性国家标准规定应当标注的其他内容。
具有包装盒的产品,还应当同时在直接接触内容物的包装容器上标注产品中文名称和使用期限。

鼓励:化妆品注册人、备案人自本公告发布之日起,按照《办法》规定对化妆品进行标签标识。
实施:自2022年5月1日起,申请注册或者进行备案的化妆品,必须符合《办法》的规定和要求。
过渡期:此前申请注册或者进行备案的化妆品,未按照本《办法》规定进行标签标识的,化妆品注册人、备案人必须在2023年5月1日前完成产品标签的更新,使其符合《办法》的规定和要求。
产品中文名称
产品中文名称应当在销售包装可视面显著位置标注,且至少有一处以引导语引出。
商标名
商标名的使用除符合国家商标有关法律法规的规定外,还应当符合国家化妆品管理相关法律法规的规定。不得以商标名的形式宣称医疗效果或者产品不具备的功效。以暗示含有某类原料的用语作为商标名,产品配方中含有该类原料的,应当在销售包装可视面对其使用目的进行说明;产品配方不含有该类原料的,应当在销售包装可视面明确标注产品不含该类原料,相关用语仅作商标名使用。
通用名
通用名应当准确、客观,可以是表明产品原料或者描述产品用途、使用部位等的文字。使用具体原料名称或者表明原料类别的词汇的,应当与产品配方成分相符,且该原料在产品中产生的功效作用应当与产品功效宣称相符。
如:商标名+烟酰胺美白面霜,配方中需含有烟酰胺,烟酰胺需具有美白功效,产品宣称美白功效。
使用动物、植物或者矿物等名称描述产品的香型、颜色或者形状的,配方中可以不含此原料,命名时可以在通用名中采用动物、植物或者矿物等名称加香型、颜色或者形状的形式,也可以在属性名后加以注明;
如:商标+隔离霜(薄荷绿),商标+保湿身体乳(玫瑰香型)
通用名、属性名 应当表明产品真实的物理状态或者形态
不同产品的商标名、通用名、属性名相同时,其他需要标注的内容应当在属性名后加以注明,包括颜色或者色号、防晒指数、气味、适用发质、肤质或者特定人群等内容;
商标名、通用名或者属性名单独使用时符合本条上述要求,组合使用时可能使消费者对产品功效产生歧义的,应当在销售包装可视面予以解释说明。
例如普通化妆品:“X美”为商标名,通用名为:白兰花精华(含白兰花油),属性名为:液
产品名称:X美白兰花精华液
因产品名称中出现了“美白”组合词,为了不让消费者对产品功效产生歧义,应该在销售包装可视面对产品名称予以解释说明
成分
化妆品标签应当在销售包装可视面标注化妆品全部成分的原料标准中文名称,以“成分”作为引导语引出,并按照各成分在产品配方中含量的降序列出。
其他微量成分(包含0.1%)
化妆品配方中存在含量不超过0.1%(w/w)的成分的,所有不超过0.1%(w/w)的成分应当以“其他微量成分”作为引导语引出另行标注,可以不按照成分含量的降序列出。
复配或者混合原料
以复配或者混合原料形式进行配方填报的,应当以其中每个成分在配方中的含量作为成分含量的排序和判别是否为微量成分的依据。
使用期限
产品使用期限应当按照下列方式之一在销售包装可视面标注,并以相应的引导语引出:
生产日期和保质期:生产日期应当使用汉字或者阿拉伯数字,以四位数年份、二位数月份和二位数日期的顺序依次进行排列标识;
生产批号和限期使用日期。
具有包装盒的产品,在直接接触内容物的包装容器上标注使用期限时,除可以选择上述方式标注外,还可以采用标注生产批号和开封后使用期限的方式。
销售包装内含有多个独立包装产品时,每个独立包装应当分别标注使用期限,销售包装可视面上的使用期限应当按照其中最早到期的独立包装产品的使用期限标注;也可以分别标注单个独立包装产品的使用期限。
其他新要求
产品执行的标准编号
化妆品标签应当在销售包装可视面标注产品执行的标准编号,以相应的引导语引出。
特殊化妆品注册证书编号
特殊化妆品:在销售包装可视面标注特殊化妆品注册证书编号,以相应的引导语引出。(特殊化妆品注册证书编号是国家药品监督管理局核发的注册证书编号)
创新用语
化妆品标签中使用尚未被行业广泛使用导致消费者不易理解,但不属于禁止标注内容的创新用语的,应当在相邻位置对其含义进行解释说明。
以免费试用、赠予、兑换等形式向消费者提供的化妆品,其标签适用本办法。
化妆品中文标签引导语示例:
产品中文名称:
净含量:
成分:
其他微量成分:
使用方法:
注意(或警告):
境内责任人:
地址:
备案人(特殊化妆品则写注册人):
地址:
生产企业:
地址:
执行标准编号:
生产日期和保质期(或生产批号和限期使用日期):
特殊化妆品注册证书编号(普通化妆品无需标注该项):
注册人或者备案人自主生产的可以简化标注为:
“注册人/生产企业:”或者“备案人/生产企业:”
化妆品净含量不大于15g或者15mL的小规格
化妆品净含量不大于15g或者15mL的小规格包装产品,仅需在销售包装可视面标注产品中文名称、特殊化妆品注册证书编号、注册人或者备案人的名称、净含量、使用期限等信息,其他应当标注的信息可以标注在随附于产品的说明书中。
具有包装盒的小规格包装产品,还应当同时在直接接触内容物的包装容器上标注产品中文名称和使用期限。
《化妆品注册备案资料管理规定》
第三十二条
存在多种销售包装的,应当提交所有的销售包装的标签图片。符合以下一种或多种情形的,提交其中一种销售包装的标签图片,其他销售包装的标签图片可不重复上传:
1.仅净含量规格不同的;
2.仅在已上传销售包装上附加标注销售渠道、促销、节日专款、赠品等信息的;
3.仅销售包装颜色存在差异的;
4.已注册或者备案产品以套盒、礼盒等形式组合销售,组合过程不接触产品内容物,除增加组合包装产品名称外,其他标注的内容未超出每个产品标签内容的;
5.通过文字描述能够清楚反映与已上传销售包装差异,并已备注说明的。
(六)产品检验报告
注册或者备案产品的产品检验报告,由化妆品注册和备案检验机构出具,应当符合《化妆品安全技术规范》《化妆品注册和备案检验工作规范》等相关法规的规定。
普通化妆品的生产企业已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证,且产品安全风险评估结果能够充分确认产品安全性的,可免于提交该产品的毒理学试验报告,有下列情形的除外:
1.产品宣称婴幼儿和儿童使用的;
2.产品使用尚在安全监测中化妆品新原料的;
3.根据量化分级评分结果,备案人、境内责任人、生产企业被列为重点监管对象的。
有多个生产企业生产的,所有生产企业均已取得所在国(地区)政府主管部门出具的生产质量管理体系相关资质认证的,方可免于提交毒理学试验报告。
(七)产品安全评估资料
《化妆品注册备案资料管理规定》
第三十四条 注册人、备案人应当按照化妆品安全评估相关技术指南的要求开展产品安全评估,形成产品安全评估报告。
必须配合仪器或者工具(仅辅助涂擦的毛刷、气垫、烫发工具等除外)使用的化妆品,应当评估配合仪器或者工具使用条件下的安全性;并应当提供在产品使用过程中仪器或者工具是否具有化妆品功能,是否参与化妆品的再生产过程,是否改变产品与皮肤的作用机理等情况的说明资料。
自2022年1月1日起,化妆品注册人、备案人申请特殊化妆品注册或者进行普通化妆品备案前,必须依据《化妆品安全评估技术导则》的要求开展化妆品安全评估,提交产品安全评估资料。
在2024年5月1日前,化妆品注册人、备案人可以按照《化妆品安全评估技术导则》相关要求,提交简化版产品安全评估报告。
自2024年5月1日前,化妆品注册人、备案人应当按照《化妆品安全评估技术导则》相关要求,提交完整版产品安全评估报告。
《化妆品安全评估技术导则》
基本要求
化妆品注册人、备案人应自行或委托专业机构开展安全评估,形成安全评估报告,并对其真实性、科学性负责。
化妆品的安全评估资料应当根据需要及时更新,保存期限不少于最后一批上市产品保质期结束以后10年。
评估人员的简历应附在评估报告之后,简历内容应包括评估人员的教育经历、化妆品相关从业经历、专业培训经历等。
化妆品产品的安全评估报告
化妆品产品的安全评估报告通常包括摘要、产品简介、产品配方、配方设计原则(仅针对儿童化妆品)、配方中各成分的安全评估、可能存在的风险物质评估、风险控制措施或建议、安全评估结论、安全评估人员签名及简历、参考文献和附录等内容。




化妆品安全评估人员的要求
1. 具有医学、药学、生物学、化学或毒理学等化妆品质量安全相关专业知识,了解化妆品成品或原料生产过程和质量安全控制要求,并具有5年以上相关专业从业经历。
2. 能查阅和分析化学、毒理学等相关文献信息,分析、评估和解释相关数据。
3. 能公平、客观地分析化妆品的安全性,在全面分析所有可获得的数据和暴露条件的基础上,开展安全评估工作,并对评估报告的科学性、准确性、真实性和可靠性负责。
4. 能通过定期接受相应的专业培训等方式,学习安全评估的相关知识,了解和掌握新的安全评估理论、技术和方法,并用于实践。